『破傷風予防に関する研究』
日本外傷学会会員各位将来計画委員会では会員および会員施設による多施設研究の支援をしています。
この度、「破傷風抗体迅速検査キット(TQS)の検証および破傷風予防に関する臨床研究」に関して研究参加の応募を開始しましたので案内申し上げます。
| 一般社団法人 日本外傷学会 将来計画委員会 委 員 長 木村 昭夫 |
研究計画書
PROTEQT (Prophylaxis of Tetanus by Quick Test) study
-迅速検査キットを使用した破傷風予防に関する研究-
- 研究目的の概要
破傷風菌は土壌中の常在菌であり、免疫を獲得していない場合や免疫能が低下した場合には、創傷などにより感染するリスクが常にある。また破傷風を一旦発症すると、10%前後の高い致死率があり、加えて長期の集中治療やリハビリテーションを必要とする例が多く、高額な医療費がかかる上に、その後の日常生活に制限が生じる症例もあり社会的損失は大きい。過去には全年齢層で相当数の破傷風の発症があった時代もあるが、現在は主にDPT(三種混合)ワクチンにより、発症は極めて少ないというレベルにまで抑えられている1)。この、安価で大きな成果をあげている予防政策の現状を鑑みると、破傷風は治療する疾患ではなく、予防すべき疾患であると言え、外傷受傷時における破傷風予防は、予防接種による能動免疫の獲得と同様に重要な課題である。
現在、我が国の予防接種事業では、DPTワクチンを一期 (生後3ヵ月~90ヵ月)の間に4回、二期(11~12歳)にDT(二種混合)ワクチンとして1回接種を勧奨するスケジュールとなっているが、破傷風抗体は終生獲得できる免疫ではなく、予防接種後約10年間は抗体価が保持されるが、その後急速に低下し、長くても20年以内と言われているため2)、欧米各国では成人以降に追加接種を推奨・実施していることが多い3)~6)。これに対して本邦では、成人以降の追加予防に関しての取り決めが明確でないため、医師が個々の判断で追加接種を行っており、予防法は個人・施設によって異なる。その要因として、破傷風発生率の低さからその診断・予防に対する医師あるいは医療機関の関心が低下していることが考えられ、また従来の破傷風免疫抗体検査は時間と費用がかかるため救急外来では殆んど行われていないことも挙げられよう。
本研究では、既に海外では実績のある破傷風抗体迅速検査キット(Tetanus Quick Stick: TQS 図1参照)7),8)を使用して迅速かつ客観的に破傷風抗体の有無を判断することが特徴である。既に本研究の前段階として当院での単施設前向き観察研究を行った結果、TQS の検査精度は海外で報告されているものと同程度であること。予防接種歴10年未満と回答した全員が十分な抗体価を有していたこと。DPT(三種混合)ワクチンが定期接種となった1968年生まれを境として抗体保有率に格段の差が生じていたことなどを報告し、それらを基にした「破傷風予防仮説アルゴリズム」を発表している9) (図2参照)。本研究において、当アルゴリズムを検証すると共に年齢別にみた抗体保有率や予防接種歴との相関などを考慮して、外傷診療における破傷風予防法の確立を目指す。
更には二次エンドポイントとして、年齢別の抗体保有率の疫学調査を兼ねるとともに、破傷風トキソイド追加接種でのブースター効果の抗体上昇率はどの程度なのか、また初期免疫完了者と非完了者ではどのような相違があるのかを検討することや、若年者に一定割合存在する低免疫抗体者の原因検討を行う予定で、将来的には救急並びに外傷診療の指針・ガイドラインなどに反映させることを目標としている。
※破傷風抗体迅速検査キット(Tetanus Quick Stick:TQS, NEPHROTEK社, FRANCE)は免疫クロマトグラフィー法を用いた試験であり、全血、血清、血漿のいずれかの検体を約30μL使用する。判定は20分後に行い、陽性の場合は、破傷風に対する十分な防御レベルである破傷風抗体価0.1 IU/mL以上を有する。 現時点では本邦未市販キットである。
- 本研究の目的
【一次エンドポイント】
- 破傷風抗体迅速検査キット(TQS)の検証
- 「破傷風予防仮説アルゴリズム」の検証 (図2参照)
- 年齢別抗体保有率の調査
- 破傷風トキソイド追加接種におけるブースター効果の検討
- 若年非免疫保持者の検討
- 研究の対象・方法
【研究デザイン】
多施設共同前向き観察研究
【研究期間】
倫理審査結果通知日 ~平成26年12月 (研究開始日より3年間の予定)
【研究対象】
対象予定数:1,600例
対象年齢:全年齢対象
対象性別:問わず
研究該当者の条件:研究施設及び関連施設を受診した外傷患者
*外傷は重症度、外傷種別に関わらず対象とする開放創のみならず、打撲等も含む
研究非該当者の条件:本研究に同意されない対象者
<サンプルサイズの設定>
これまでの文献7),8)からTQS陽性の場合、破傷風に対する十分な防御レベルである血清破傷風抗体価0.1 IU/ml以上を有すると言われ、従来の破傷風抗体検査であるELISA法に対するTQSの感度は70~90.4% 、特異度は87.2~98.0% 、陽性的中率92.1%と高い診断率が報告されている8)。TQSの感度を0.7、特異度を0.95と仮定し、2区分変数を用いて記述的研究を行う場合の必要サンプルサイズ(N)の計算式:『N=4Zα2P(1-P)÷W2』より
・感度の期待割合を0.7と仮定
期待割合(P)=0.7、信頼区間幅(W)=0.05、信頼水準=95%(α=0.05)
Zα:信頼水準が(1-α)のとき両側αに対する標準正規偏差(α=0.05ではZα=1.96)
上記の値を一般式に当てはめると、4×1.962×0.7(1-0.7)÷0.052≒1,291
・特異度の期待割合を0.95と仮定
期待割合(P)=0.95、信頼区間幅(W)=0.05、信頼水準=95%(α=0.05)
Zα:信頼水準が(1-α)のとき両側αに対する標準正規偏差(α=0.05ではZα=1.96)
上記の値を一般式に当てはめると、4×1.962×0.95(1-0.95)÷0.052≒292
上記より感度・特異度の計算式上の数字を合計すると1291+292=1,583例だが、不備例や症例の偏り等を考慮してサンプルサイズを1,600例と設定した。
<具体的手順>
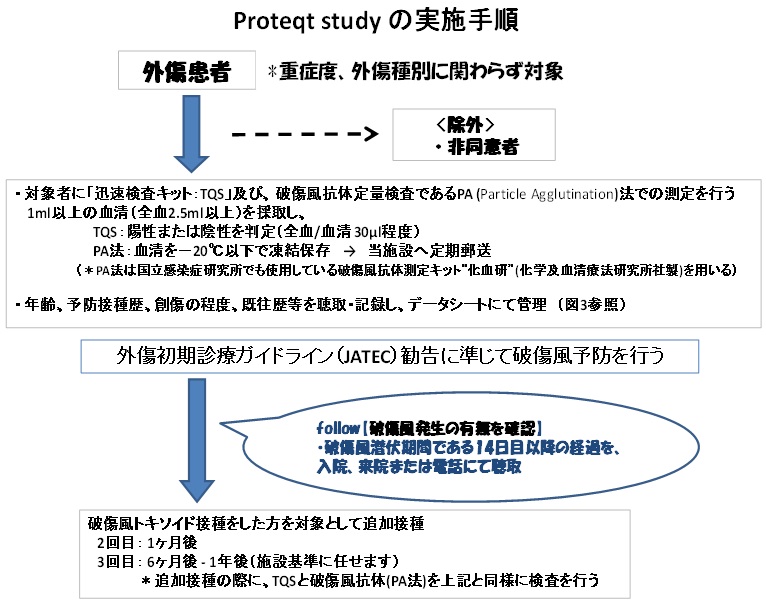
- 研究における倫理的配慮
- 研究の対象とする個人の人権の擁護
使用した試料(血液)は検査後に全て廃棄。また、保有する個人情報や検査に関する情報は研究代表者が安全に管理して、個人を特定する形での第三者への公表は絶対にせず、プライバシーを最大限に尊重する。 - 被験者に理解を求め同意を得る方法
研究代表者、又は協力者が同意説明文書を用いて本人(もしくは意識障害等にて本人が同意・署名できない場合には代諾人)に口頭にて説明を行い、本研究の趣旨を理解して頂いた上で同意書に署名して頂く。 - 研究によって生じる個人の不利益と医学上の利益または貢献度の予測
本研究は臨床観察研究のため、検査結果如何によって治療が変更されることはなく、個人が不利益を被ることはない。また、抗体保有率の現状を考慮すると不必要な予防が行われている可能性や、反対に予防投与が必要な場合に投与されていない可能性が高いと思われる現状を、対費用効果も含めた救急外来における破傷風予防アルゴリズムを確立することで改善できることが期待される。
【同意書について】
サインされた同意書を、研究該当者すべてに要求する。 - 研究の対象とする個人の人権の擁護
- データの集積法と保管
図3に示した様なデータシートを用いて、電子端末に匿名化されている臨床情報のみの集積を徹底化し、解析を進める計画である。国際医療研究センター病院で測定される破傷風抗体定量検査(PA法)の結果以外は各施設で入力する。すべての研究に関する記録は、主たる研究者の責任で鍵のかかる部位に保管する。 - 利益相反、 研究に係る費用等
【利益相反】
本研究を行う上で、如何なる企業・団体等と産学官連携活動その他の社会貢献活動を行うこと や、一定額以上の物品や金品、サービスを受け取ること、役務提供を受けることは一切ない。
【費用負担】
平成22年度国際医療研究委託事業研究費より支出予定
【補償】
本研究は臨床観察研究のため、検査結果の如何によって治療が変更されることはなく、個人が不利益を被ることは決してない。
【研究の中止】
観察研究のため、基本的には研究期間中の中止はしない予定だが、対象となる被験者は、検査の開始前・開始後に関わらず、本研究の同意をいつでも撤回できる。また、同意を撤回した場合、試料やデータは全て廃棄する。 - 手法の変更に関して
委員会の承認なしに研究手法や薬剤の変更は行わない。
変更を要する場合は、連絡を取り、再度承認を得る。 - 研究のレビュー
毎年研究の進み具合、対象件数等を報告する。
<参考文献>
1) 福田靖, 岩城正昭, 高橋元秀:破傷風.国立感染症研究所 病原微生物検出情報 (Infectious diseases Surveillance Report: IASR) 2002;23:1-9.
2) Rhee P, et al: Tetanus and trauma: a review and recommendations. J trauma 2005; 58: 1082-88.
3) Department of Health. Chapter 30: Tetanus. In: Immunisation against Infectious Disease[Online]. London: HMSO, 2006. 367-384.
4) Canadian Medical Association (2002). In Canadian Immunization Guide. Sixth edition. Canadian Medical Association [Online]. Ontario: Her Majesty the Queen in Right of Canada, 2003. 208-213
5) The National Health and Medical Researchth Edition Council. The Australian Immunisation Handbook-8th edition [Online]. Canberra: National Capital Printers, 2003. 234-239.
6) Recommended Adult Immunization Schedule-United States, October 2006-September 2007. The Centers for Disease Control and Prevention: Morbidity and Mortality Weekly Report. 2006; 55: Q1-Q4.
7) Stubbe M, et al. ; Seroprotection against tetanus in patients attending an emergency department in Belgium and evaluation of a bedside immunotest. Eur J Emerg Med. 2007 Feb; 14(1):14-24.
8) Elkharrat, D et al. Incorporation of a rapid test into the current French Ministry of Health National Framework in order to optimize the antitetanus prophylaxis offered in wound management by accident & emergency departments. Medecine et maladies infectieuses March 2005; 35: 323-328.
9) 我が国における新たな破傷風予防アルゴリズムの提唱 ‐第一報‐第38回日本救急医学会報告.








